RET是一个原癌基因,全名:RET proto-oncogene,其位于10号染色体上,激活下游信号通路STAT/PLCγ,促进细胞的存活、迁移和生长等。此基因在神经脊发育中起重要作用,并且由于细胞遗传学的重排原因,在体内和体外均产生致癌性的激活。
RET与肿瘤的关系
目前已报道的RET在癌症中异常活化的机制:
- RET基因本身的突变
- 框内RET基因融合,即RET基因和其他基因拼接在一起,包括与KIF5B、CCDC6、TRIM33等基因的融合突变
- RET基因的异常超表达
其中RET融合和突变共约占RET基因变异的70%,是RET的致癌性活化主要的两种机制。
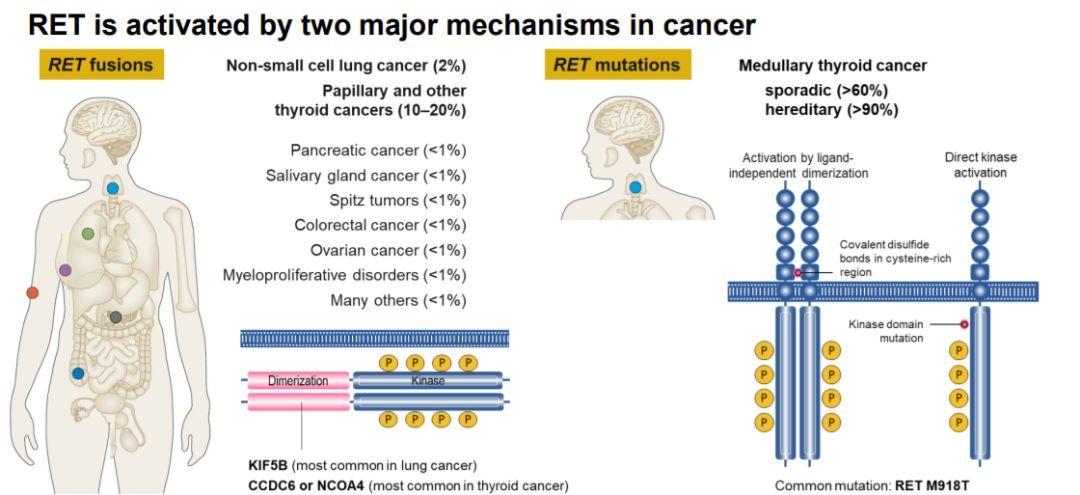
(不同类型的肿瘤中RET突变和融合的发生率) RET突变在非小细胞肺癌(NSCLC)中约占1%~2%,属于较为罕见的突变,且RET突变具有较强的排他性,能够独立驱动非小细胞肺癌的发病,很少与EGFR、KRAS、ALK、HER2、BRAF等其他驱动基因同时存在。在肺癌中,RET融合突变更常见于无吸烟史、年轻的女性患者,致病类型主要为腺癌,其特点为原发病灶直径较小(通常<3 cm)等。 (NSCLC、non-MTC和其他实体瘤推荐RET检测的路径) 除了RET融合检测外,其他实体瘤患者可能还需要根据待定临床试验的结果进行RET突变检测,最好通过NGS来完成,如果NGS不可及,可以使用Q-PCR。 产品应用: 更多肿瘤融合FFPE标准品相关信息
RET的靶向之路
由于RET和VEGFR2高度同源,早前RET患者可选择的靶向药物并不多。在千呼万唤和多个全球性临床研究中,新型RET选择性抑制剂塞尔帕替尼(Selpercatinib,LOXO-292)和普拉替尼(Pralsetinib,BLU-667)因在晚期RET融合阳性NSCLC中显示出优越的抗肿瘤活性和安全性,已分别于2020年5月和2020年9月获FDA批准上市。
2021年3月24日普拉替尼也获得中国国家药监局(NMPA)批准,作为国家一类新药用于接受过含铂化疗的RET融合NSCLC患者的治疗,成为国内第一个获批的高选择性RET抑制剂。
由于我国NSCLC患者的基数庞大,RET融合阳性患者的绝对数量非常大,所以普拉替尼的获批对于中国患者的意义非凡。
关于RET融合/突变的检测
不同的诊断方法已被用于检测RET基因组改变的存在,例如IHC、FISH、RNA和基于DNA的NGS分析,然而,IHC的敏感性和特异性并非最佳,所以IHC不能被视为一种可靠的检测方式。
对于非小细胞肺癌(NSCLC)、甲状腺非髓样癌(non-MTC)或其他实体肿瘤: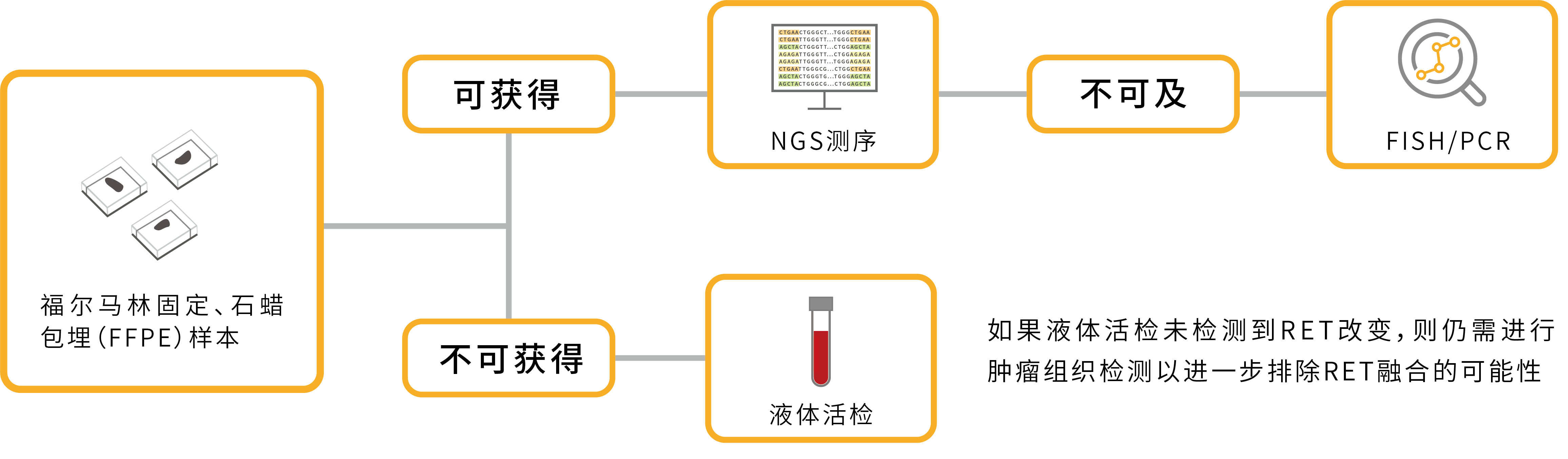
目前对RET基因融合检测的推荐已经在很多国内外指南和共识中有所体现:
提高检测质控意识,规范RET相关基因检测
在临床实践中,多种检测方式已应用于检测RET基因融合,但灵敏度和特异度不同,各具有优缺点。目前RET检测临床应用最多的是NGS和PCR,FISH则作为第二平台的验证非常重要。
NGS检测分为DNA和RNA水平,RET在 DNA层面上检测敏感性几乎可以达到100%,但是部分研究中也存在漏检,其他一些罕见融合存在假阳性的问题;RNA层面的检测虽然方便,但是RNA的质量和数量也会影响到检测结果。
PCR可以实现联合检测,通过提取RNA进行多基因检测,尽管PCR非常方便快速,也存在以下缺点:
随着普拉替尼的获批,临床检测会越来越多,RET融合检测亟需规范化。
为了指导临床检测获得准确的结果,使患者得到最大限度的获益,《中国非小细胞肺癌RET基因融合临床检测专家共识》中除了分析常用RET基因融合检测方法和判读标准外,也对其检测流程阐述了注意事项及做好室内外质控的规范化要求:
菁良解决方案
菁良基因的肿瘤融合FFPE标准品,包含RT-PCR验证的融合表达位点,及数字PCR验证的基因融合位点,成品为福尔马林固定,石蜡包埋处理的FFPE切片,主要用于基因融合检测流程的质量控制和性能验证。
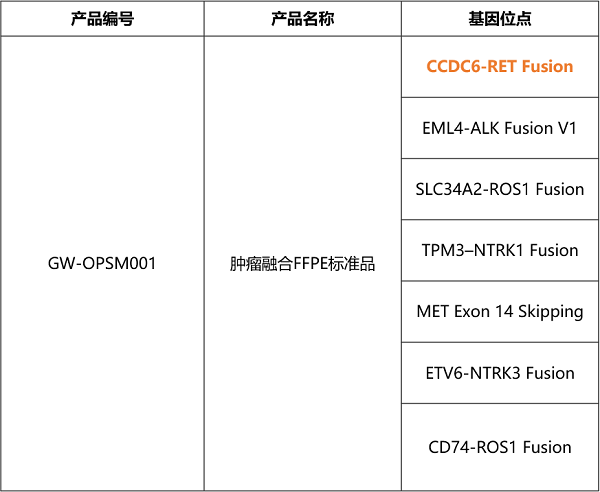
PCR及NGS平台皆适用
DNA及RNA提取效率的验证
基因融合检测panel的性能验证和日常质控
基因融合检测实验室室内及室间质评
可点击“www.gene-well.com”查看
更多融合基因需求支持个性化定制
